

BNP NT-proBNP
分子量約3,500 約8,500
ホルモン活性+ -
交叉性proBNP,BNP proBNP,NT-proBNP
半減期約20分約120分
クリアランスNPR-A,NPR-C,NEP,腎臓腎臓
採血法EDTA加血漿血清/ヘパリン加/EDTA加血漿
添付文書記載基準値≦18.4 pg/mL ≦55 pg/mL
分子量約3,500 約8,500
ホルモン活性+ -
交叉性proBNP,BNP proBNP,NT-proBNP
半減期約20分約120分
クリアランスNPR-A,NPR-C,NEP,腎臓腎臓
採血法EDTA加血漿血清/ヘパリン加/EDTA加血漿
添付文書記載基準値≦18.4 pg/mL ≦55 pg/mL
1 慢性心不全と神経体液因子
① 交感神経系
心不全では,血行動態変化によって動脈および心肺圧受容器を介する求心性の交感神経抑制信号が低下する.一方,心房や肺静脈壁からの交感神経求心路を介して交感神経が亢進する.さらに心臓交感神経求心路を介する反射も正常より亢進している.肺や腎のうっ血が生じるとノルエピネフリンのクリアランスが低下し,結果的に血漿ノルエピネフリンが増加する.心不全では筋交感神経活動も亢進するが,これは血管運動中枢自体の亢進を反映している.慢性心不全患者にしばしばみられるCheyne-Stokes呼吸時には,無呼吸時に一致して交感神経活動の亢進がみられる.このような交感神経の亢進は,急性心不全時には重要な代償機転として働くが,亢進が慢性化すると心臓の負荷を増大し,不整脈誘発や直接的心筋障害を来たし心機能を悪化させる.
Cohnは血漿ノルエピネフリン濃度が生命予後の指標になること30),さらにノルエピネフリンの増加を抑制すると長期予後が改善する可能性を示した.その後,実際
にβ遮断薬が心不全患者の予後を改善することを実証した大規模臨床試験が数多く報告されるようになった.血漿ノルエピネフリン濃度は全身の交感神経指標であ
り,心不全では,心臓交感神経活性の評価が有用であり,この評価指標として,ノルエピネフリンのアナログを用いたMIBGシンチが用いられる.
② レニン・アンジオテンシン・アルドステロン(RAA)系
心不全ではRAA系が賦活され,アンジオテンシンⅡが過剰に産生される.軽度の心機能障害でも血漿レニン活性値が上昇している例があり,また重症心不全症例のすべてに血漿レニン活性値が上昇しているとは限らない.SAVE試験においても血漿レニン活性値,ノルエピネフリン,バソプレシン,ANPは正常から高値まで広
い範囲にわたり,各神経体液因子間には相関は認められなかった31).それにもかかわらず,ACE阻害薬,アンジオテンシンⅡ受容体拮抗薬(ARB)が心不全患者の
症状,心機能,生存率を改善する.このことは循環RAA系とは独立に組織 RAA系が賦活化され,心臓のリモデリングに関与していることを示唆している32),33).
一方,ACE阻害薬投与にもかかわらず,投与初期には低下していたアルドステロンの血中濃度が再び増加してくるブレイクスルー現象が指摘されている34).
アルドステロン自体も腎臓でのナトリウム貯留,マグネシウムやカリウム喪失を惹起する作用の他,交感神経亢進,副交感神経抑制,圧受容器の機能異常等を引き起こす.心臓,特に不全心や血管に働いて,心筋の線維化,血管障害に直接関与しているとの臨床的実験的知見が集積されてきている35)-37).また,不全心ではレニンやアンジオテンシンⅡのみならずアルドステロンも心臓で産生されるという報告と36),心臓局所で産生されているよりも循環血中のアルドステロンが心臓に摂取されて機能しているとの報告がある35).RALES 試験においてアルドステロン拮抗薬のスピロノラクトンは重症心不全で,死亡率を30%減少させ38),さらにEPHESUS試験39)では,ACE阻害薬やβ遮断薬等の標準治療を受けた急性心筋梗塞患者において,アルドステロン受容体特異的拮抗薬であるエプレレノンが死亡率を15%減少させたことが報告された.RALES試験38)やEPHESUS試験39)の結果,慢性心不全や急性心筋梗塞患者において,ACE阻害薬やβ遮断薬等の標準治療薬に抗アルドステロン薬を併用することが生命予後の改善につながることが証明された.抗アルドステロン薬が予後改善効果を示した理由の1 つに,左室リモデリング改善効果が考えられる40),41).ACE阻害薬やARB投与下においてもアルドステロン-ブレイクスルー現象が認められること34),アルドステロンはACTH,エンドセリン,K,ANP,BNP等によっても制御されていること等から,従来の心不全治療薬にアルドステロンの分泌を抑制する薬剤やミネラロコルチコイド受容体阻害薬の併用が有用である.RALES,EPHESUS試験の結果をふまえて,抗アルドステロン薬の作用機序の検討により,心筋線維化の指標としてⅠ型,Ⅲ型プロコラーゲン濃度40)-44)や,ミネラロコルチコイド受容体刺激作用を有するコーチゾール濃度42)-44)等のバイオマーカーの有用性が報告されている.今後は,抗アルドステロン薬の作用機序の解明と,拡張不全による心不全治療における抗アルドステロン薬の有用性についての解明が期待される.ヒト心不全における非ACEを介するアンジオテンシンⅡ産生の臨床的な意義に関しては今後の検討を要する45),46).
③ ナトリウム利尿ペプチド
1)ナトリウム利尿ペプチドの概要
ナトリウム利尿ペプチドには ANP,BNP,CNP(C型ナトリウム利尿ペプチド)がある.ANPは主として心房で,BNPは主として心室で合成される心臓ホルモンであり,血中を循環している47).ANPは心房の伸展刺激により,BNPは主として心室の負荷により分泌が亢進し,血中濃度が上昇する.つまり,ANPやBNP,特にBNPは心室への負荷の程度に鋭敏に反映する生化学マーカーである48)-51).CNPは神経ペプチドとして中枢神経系にも存在する他,血管内皮細胞や単球・マクロファージでもその発現が確認され,血管壁ナトリウム利尿ペプチド系の主たるリガンドである.
培養心筋細胞に,伸展刺激,カルシウム負荷,アンジオテンシンⅡ,エンドセリン,LIF,カルディオトロフィン,IL1-β等で刺激するとBNP遺伝子発現は亢進する52),53).したがって,血中BNP濃度が上昇している時には,逆に細胞レベルで考えると,心臓局所で伸展刺激や液性因子による刺激が活性化していると考えられる.
ANP,BNPは,利尿,ナトリウム利尿,血管拡張,アルドステロン分泌抑制作用,さらに心臓局所では心筋肥大抑制,心筋線維化抑制作用を有している.これらの
働きは特に,アンジオテンシンⅡのタイプ1 型(AT1)受容体を介する作用とあらゆる部位で機能的に拮抗しており,ANP/BNPの心保護作用が期待されている.実際
に,我が国では急性心不全治療薬としてANP(hANP)が,米国では,BNPが用いられている.ANP,BNP治療による心筋保護作用は,ニトログリセリンとの比較で
急性心筋梗塞後の左室リモデリング抑制効果54)や心事故の改善効果55),カテコルアミンとの比較で短期予後改善効果56)が認められている.慢性心不全患者に
おいても有用性と予後改善効果が期待されるが57)今後の検討が必要である.心不全で,血中ANP・BNP濃度が上昇しているもう1 つの原因として,ANP,BNPの
クリアランスが遅延していることである.ANP,BNPは受容体(NPR-A,NPR-B)に結合した後に内部化によって分解される場合と,中性エンドペプチダーゼ(NEP)によって分解される場合が知られている. 代謝と病態との関係はまだ十分には解明されていないが,腎機能低下によりクリアランスが低下することが報告されている58)-60).腎機能低下による影響は,分子量の大きいBNP前駆体のN端側フラグメント(NT-proBNP)の方がBNPより受けやすいと考えられる.
2)BNP を利用した慢性心不全の診断と重症度評価
心不全の適切な治療の為には,迅速かつ正確な診断が不可避であるが,慢性心不全,特に代償期の心不全や,プライマリーケアにおける心不全の診断は必ずしも容易ではない.呼吸器疾患,関節疾患,肥満,静脈瘤患者も心不全患者と誤診されることがある.慢性心不全の補助診断法としてのナトリウム利尿ペプチド,特にBNPの有用性を示す論文が多く報告されている.血中ANP濃度やBNP濃度は血行動態とよく相関するが,BNPのほうが左室拡張末期圧をよく反映し,心不全の補助診断法としてBNPの方が感受性,特異度の双方でANPより優位であるという報告が多い49),60).BNPが心不全の補助診断法として特に優れているのは,(1)心不全の存在診断,(2)心不全の重症度診断,(3)心不全の予後診断である.
プライマリーケアにおいてのみならず,呼吸困難で受診した患者において心不全の臨床診断(収縮機能障害,拡張機能障害)に血中BNP濃度測定が有用であること
が報告されている61),62).呼吸困難で救急来院した症例約1,500例を対象にした検討では,BNPが,問診や身体所見,X線所見等の診断パラメターのなかで最も有用であった61)(この研究ではBiosite製のBNP測定装置を用いてカットオフ値を設定しているが,シオノリアBNPとの換算式が確定していない現在では,その値を直接我が国にあてはめることはできない).血中BNP濃度はNew York Heart Association(NYHA)重症度分類に平行して上昇し,BNP値が高いほど心不全が存在し
重症である.
また,BNP濃度(NT-proBNPも含む)と予後の関係については,最初は重症心不全患者において報告され63),海外の大規模臨床試験のサブ解析においても確認
された64),65).重症慢性心不全患者を対象にARBの有用性を検討したVal-HeFT研究のサブ解析では,すべての症例をBNP値の低い順に4分割すると,BNPの高い群ほど心事故の発生率の高いことが示された.この研究での中央値は97 pg/mL(この研究ではシオノリアBNPで測定されており,我が国と同じ測定系である)であり,BNP値が10 pg/mL上昇するごとに死亡率が1.2%上昇することが報告されている64).また,慢性心不全患者を年間追跡した臨床研究では,ANP,BNP,ノルエピネフリン,臨床症状,血行動態所見を比較して,予後との関連を調べ,BNP濃度と肺動脈楔入圧のみがそれぞれ単独で予後規定因子であることが報告されている63).慢性心不全で入院した症例を対象に,退院時のBNP値で退院後の心事故(死亡,心不全の悪化による再入院)の発生率を前向きに比較検討すると,BNP値が低いほど有意に低率であり,およそ200~ 250 pg/mLが退院時のメルクマールになる66).さらには,外来通院中の安定した患者においては,190 pg/mL以上で心事故が増加する67).また,心筋梗塞後の患者においては180 pg/mL以上(約1か月の測定)で心臓死が増加すると報告されている68).
一般集団を対象にした健診におけるBNPの有用性に関しては未だ結論が出ていない.ただ,Framingham Studyでは集団の80パーセンタイル値(約20 pg/mL; シ
オノリアBNPで測定)以上の群では,以下の群より有意に心事故の発生率が高いことが示されている69).心不全の場合,陰性的中率が高いので,呼吸困難等で心不全を疑うべき症例において,BNP値が正常であれば,心不全である可能性は極めて低い.
我が国では主にBNPの血中濃度が測定されているが,欧米ではBNP前駆体のNT-proBNPの測定系もよく利用されており,心不全の診断・予後診断にBNPとほぼ同等の結果が報告されている70),71).両者の特徴を表3に示すが,使い分ける際には注意が必要である.BNPには生理活性があり,NT-proBNPには生理活性が
ないこと,半減期が長いこと,腎機能の影響を受けやすいこと等が特徴である.
BNPやNT-proBNPを利用した心不全診断と重症度評価をする上での問題点は,年齢,性別,肥満,腎機能等の影響を受けることである.BNP,NT-proBNPの測定
系の世界的標準化とともにこれらの問題点解決が期待される.
④ その他の神経体液因子
1)エンドセリン
エンドセリン(ET)は1988年に血管内皮細胞培養上清中から発見された72)強力で,かつ持続的な血管平滑筋収縮性ペプチドである.エンドセリンは,構造と薬理活
性の異なる3種類のアイソペプチド,ET-1,ET-2,ET-3からなるETファミリーである.ET受容体にはET-1 選択性のET-A受容体,およびETアイソペプチド非選択性ET-B受容体がある.血管平滑筋にはET-A受容体が発現し,血管収縮に働く.一方,血管内皮細胞においては,ET-B受容体が発現してNOの放出に関与する.血管平滑筋にもET-B受容体が発現して収縮に関与するとされている.ET-B受容体はアルドステロンの分泌にも関与する73).
心不全の重症度が増すにつれて,血漿ET-1 濃度は高値を示すが74),特にNYHAの重症度分類Ⅳ度で上昇する.血漿ET-1,big-ET-1 濃度はLVEFとは逆相関して,死亡率の規定因子の1つである75)-77).慢性心不全患者を対象に,ACE阻害薬やβ遮断薬との併用でET受容体拮抗薬の有効性が検討されたが,現時点では予後改善効果はない.血中のET-1 は肺循環から,また末梢循環からも産生され,肺血管床ではET-1 の産生量と肺血管抵抗とは正の相関を示すことから,肺高血圧に関係している74).現在,肺動脈性肺高血圧症におけるET-A/B受容体拮抗薬,ボセンタンの臨床応用が可能であるが,心不全治療薬としては確立されていない.
2)アドレノメデュリン
アドレノメデュリン(AM)は,心不全の重症度が増すにつれて血中濃度は増加し,予後不良と関係する78).ANP,BNPに比較して79),心不全の重症度評価,治療
効果判定の指標にはなりにくい.AMはIL-1,TNF-α等のサイトカインにより分泌を刺激され,心臓のみならず全身の血管床から産生され,オートクリン,パラクリンに細胞保護的に働いている.AMは細胞内cAMPを増加することで,血管拡張作用,心機能改善作用,神経体液因子調節作用もあるので心不全治療薬として有用である
可能性がある78).
3)バゾプレッシン
バゾプレッシンは脳下垂体後葉から分泌されるホルモンで,心不全で上昇しV1受容体を介して血管収縮,V2受容体を介して体液調節をしている.バゾプレッシンの
前駆体のフラグメントであるコペプチン濃度は,心不全患者で予後と関連すると報告されている80).バゾプレッシン受容体の拮抗薬の臨床効果の検討がされた結果,V2受容体拮抗薬は,利尿効果において有用性が認められたが81),予後改善効果は認められなかった.
⑤ その他のバイオマーカー
1)心筋傷害マーカー
心筋梗塞のバイオマーカーでもある心筋特異的トロポニン(I,T)濃度が,虚血性心疾患でのリスク指標としての有用性は確立されているが,非虚血性心筋疾患でも
上昇することが指摘され,持続的な上昇が予後不良の指標となる可能性が指摘されている82)-84).最近,高感度トロポニン濃度測定系が,従来の測定系に比べて,急性冠症候群の診断に有用であるとの報告もあり85),86),その慢性心不全のリスク評価での有用性が期待される87),88).
2)炎症性マーカー
心不全の発症に免疫細胞,およびそれらが産生するサイトカインの関与が指摘されている89).実際,心不全患者においてtumor necrosis factor-α(TNF-α),Interleukin-6(IL-6)が血中に増加し,予後とも関係する90),91).これらのサイトカインは直接的な陰性変力作用,β受容体に対する反応抑制,一酸化窒素の産生を介する心筋細胞障害によって心機能を抑制する.さらに筋肉の疲弊を来たし心臓悪液質にも関与する.また血管の透過性亢進,末梢血管抵抗増大,心不全患者の運動耐容能低下にも関与する.TNF-α,IL-6等のサイトカイン以外にも可溶性サイトカイン受容体92)ならびに可溶性接着分子も増加している75).なかでも,高感度CRP濃度測定が基礎疾患の有無にかかわらず予後と関連しているとの報告がある93),94).高感度CRP測定は,サイトカインより簡便で,安価であるが特異性に欠ける.
3)酸化ストレスマーカー
心不全では,酸化ストレスが亢進し,内皮障害や心機能障害増悪の要因とされる.その指標として,血中酸化LDL濃度95),96), 血中- 尿中8-iso-prostaglandin PGF2α(isoprostane)97),や8-OH-deoxyguanosine98),99)等が報告されている.酸化ストレス亢進は,交感神経系やRAA系,炎症性反応等の経路の下流に位置すると考えらるが,多臓器不全を合併する心不全では,その由来細胞や臓器が特定できない点が問題である.尿酸高値は,非特異的な指標ではあるが,簡便な酸化ストレスマーカーとして有用である可能性がある100)-102).
4)アディポサイトカイン
メタボリック症候群は,虚血性心疾患の危険因子であり心不全のリスクでもある.メタボリック症候群関連アディポサイトカインの1つであるアディポネクチン濃度は心不全で上昇し,予後と関連すると報告されている103)-105).アディポネクチンには,抗動脈硬化作用,インスリン抵抗性改善作用があり,心不全のない患者においてはアディポネクチン低値が心筋梗塞発症のリスクとされる.一方,心筋梗塞や心不全を発症するとアディポネクチン濃度は上昇し,予後不良の指標となる.この現象
は,肥満が心不全のリスクであるが,心不全患者において肥満患者の予後は比較的良好で,やせ(悪液質)患者で予後不良である(オベシティパラドックス)のと似た現象である.
神経体液因子の評価
ClassⅠ
● 血漿BNP濃度測定:診断,重症度,予後評価
ClassⅡ a
● 血漿BNP濃度測定:治療効果判定
● NT-proBNP濃度測定:診断,重症度,予後評価
● 血漿ノルエピネフリン濃度測定:重症度,予後評価
● 心筋トロポニン濃度測定:重症度,予後評価
● 血漿ANP濃度測定
● 血漿レニン活性値,または濃度測定
● 血漿アルドステロン濃度測定
ClassⅡb
● NT-proBNP濃度測定:治療効果判定
● 血漿BNP濃度やNT-proBNP濃度測定:スクリーニング目的として
ClassⅢ
● スクリーニング目的での神経体液因子(血漿BNP濃度,NT-proBNP濃度を除く)
心不全では,血行動態変化によって動脈および心肺圧受容器を介する求心性の交感神経抑制信号が低下する.一方,心房や肺静脈壁からの交感神経求心路を介して交感神経が亢進する.さらに心臓交感神経求心路を介する反射も正常より亢進している.肺や腎のうっ血が生じるとノルエピネフリンのクリアランスが低下し,結果的に血漿ノルエピネフリンが増加する.心不全では筋交感神経活動も亢進するが,これは血管運動中枢自体の亢進を反映している.慢性心不全患者にしばしばみられるCheyne-Stokes呼吸時には,無呼吸時に一致して交感神経活動の亢進がみられる.このような交感神経の亢進は,急性心不全時には重要な代償機転として働くが,亢進が慢性化すると心臓の負荷を増大し,不整脈誘発や直接的心筋障害を来たし心機能を悪化させる.
Cohnは血漿ノルエピネフリン濃度が生命予後の指標になること30),さらにノルエピネフリンの増加を抑制すると長期予後が改善する可能性を示した.その後,実際
にβ遮断薬が心不全患者の予後を改善することを実証した大規模臨床試験が数多く報告されるようになった.血漿ノルエピネフリン濃度は全身の交感神経指標であ
り,心不全では,心臓交感神経活性の評価が有用であり,この評価指標として,ノルエピネフリンのアナログを用いたMIBGシンチが用いられる.
② レニン・アンジオテンシン・アルドステロン(RAA)系
心不全ではRAA系が賦活され,アンジオテンシンⅡが過剰に産生される.軽度の心機能障害でも血漿レニン活性値が上昇している例があり,また重症心不全症例のすべてに血漿レニン活性値が上昇しているとは限らない.SAVE試験においても血漿レニン活性値,ノルエピネフリン,バソプレシン,ANPは正常から高値まで広
い範囲にわたり,各神経体液因子間には相関は認められなかった31).それにもかかわらず,ACE阻害薬,アンジオテンシンⅡ受容体拮抗薬(ARB)が心不全患者の
症状,心機能,生存率を改善する.このことは循環RAA系とは独立に組織 RAA系が賦活化され,心臓のリモデリングに関与していることを示唆している32),33).
一方,ACE阻害薬投与にもかかわらず,投与初期には低下していたアルドステロンの血中濃度が再び増加してくるブレイクスルー現象が指摘されている34).
アルドステロン自体も腎臓でのナトリウム貯留,マグネシウムやカリウム喪失を惹起する作用の他,交感神経亢進,副交感神経抑制,圧受容器の機能異常等を引き起こす.心臓,特に不全心や血管に働いて,心筋の線維化,血管障害に直接関与しているとの臨床的実験的知見が集積されてきている35)-37).また,不全心ではレニンやアンジオテンシンⅡのみならずアルドステロンも心臓で産生されるという報告と36),心臓局所で産生されているよりも循環血中のアルドステロンが心臓に摂取されて機能しているとの報告がある35).RALES 試験においてアルドステロン拮抗薬のスピロノラクトンは重症心不全で,死亡率を30%減少させ38),さらにEPHESUS試験39)では,ACE阻害薬やβ遮断薬等の標準治療を受けた急性心筋梗塞患者において,アルドステロン受容体特異的拮抗薬であるエプレレノンが死亡率を15%減少させたことが報告された.RALES試験38)やEPHESUS試験39)の結果,慢性心不全や急性心筋梗塞患者において,ACE阻害薬やβ遮断薬等の標準治療薬に抗アルドステロン薬を併用することが生命予後の改善につながることが証明された.抗アルドステロン薬が予後改善効果を示した理由の1 つに,左室リモデリング改善効果が考えられる40),41).ACE阻害薬やARB投与下においてもアルドステロン-ブレイクスルー現象が認められること34),アルドステロンはACTH,エンドセリン,K,ANP,BNP等によっても制御されていること等から,従来の心不全治療薬にアルドステロンの分泌を抑制する薬剤やミネラロコルチコイド受容体阻害薬の併用が有用である.RALES,EPHESUS試験の結果をふまえて,抗アルドステロン薬の作用機序の検討により,心筋線維化の指標としてⅠ型,Ⅲ型プロコラーゲン濃度40)-44)や,ミネラロコルチコイド受容体刺激作用を有するコーチゾール濃度42)-44)等のバイオマーカーの有用性が報告されている.今後は,抗アルドステロン薬の作用機序の解明と,拡張不全による心不全治療における抗アルドステロン薬の有用性についての解明が期待される.ヒト心不全における非ACEを介するアンジオテンシンⅡ産生の臨床的な意義に関しては今後の検討を要する45),46).
③ ナトリウム利尿ペプチド
1)ナトリウム利尿ペプチドの概要
ナトリウム利尿ペプチドには ANP,BNP,CNP(C型ナトリウム利尿ペプチド)がある.ANPは主として心房で,BNPは主として心室で合成される心臓ホルモンであり,血中を循環している47).ANPは心房の伸展刺激により,BNPは主として心室の負荷により分泌が亢進し,血中濃度が上昇する.つまり,ANPやBNP,特にBNPは心室への負荷の程度に鋭敏に反映する生化学マーカーである48)-51).CNPは神経ペプチドとして中枢神経系にも存在する他,血管内皮細胞や単球・マクロファージでもその発現が確認され,血管壁ナトリウム利尿ペプチド系の主たるリガンドである.
培養心筋細胞に,伸展刺激,カルシウム負荷,アンジオテンシンⅡ,エンドセリン,LIF,カルディオトロフィン,IL1-β等で刺激するとBNP遺伝子発現は亢進する52),53).したがって,血中BNP濃度が上昇している時には,逆に細胞レベルで考えると,心臓局所で伸展刺激や液性因子による刺激が活性化していると考えられる.
ANP,BNPは,利尿,ナトリウム利尿,血管拡張,アルドステロン分泌抑制作用,さらに心臓局所では心筋肥大抑制,心筋線維化抑制作用を有している.これらの
働きは特に,アンジオテンシンⅡのタイプ1 型(AT1)受容体を介する作用とあらゆる部位で機能的に拮抗しており,ANP/BNPの心保護作用が期待されている.実際
に,我が国では急性心不全治療薬としてANP(hANP)が,米国では,BNPが用いられている.ANP,BNP治療による心筋保護作用は,ニトログリセリンとの比較で
急性心筋梗塞後の左室リモデリング抑制効果54)や心事故の改善効果55),カテコルアミンとの比較で短期予後改善効果56)が認められている.慢性心不全患者に
おいても有用性と予後改善効果が期待されるが57)今後の検討が必要である.心不全で,血中ANP・BNP濃度が上昇しているもう1 つの原因として,ANP,BNPの
クリアランスが遅延していることである.ANP,BNPは受容体(NPR-A,NPR-B)に結合した後に内部化によって分解される場合と,中性エンドペプチダーゼ(NEP)によって分解される場合が知られている. 代謝と病態との関係はまだ十分には解明されていないが,腎機能低下によりクリアランスが低下することが報告されている58)-60).腎機能低下による影響は,分子量の大きいBNP前駆体のN端側フラグメント(NT-proBNP)の方がBNPより受けやすいと考えられる.
2)BNP を利用した慢性心不全の診断と重症度評価
心不全の適切な治療の為には,迅速かつ正確な診断が不可避であるが,慢性心不全,特に代償期の心不全や,プライマリーケアにおける心不全の診断は必ずしも容易ではない.呼吸器疾患,関節疾患,肥満,静脈瘤患者も心不全患者と誤診されることがある.慢性心不全の補助診断法としてのナトリウム利尿ペプチド,特にBNPの有用性を示す論文が多く報告されている.血中ANP濃度やBNP濃度は血行動態とよく相関するが,BNPのほうが左室拡張末期圧をよく反映し,心不全の補助診断法としてBNPの方が感受性,特異度の双方でANPより優位であるという報告が多い49),60).BNPが心不全の補助診断法として特に優れているのは,(1)心不全の存在診断,(2)心不全の重症度診断,(3)心不全の予後診断である.
プライマリーケアにおいてのみならず,呼吸困難で受診した患者において心不全の臨床診断(収縮機能障害,拡張機能障害)に血中BNP濃度測定が有用であること
が報告されている61),62).呼吸困難で救急来院した症例約1,500例を対象にした検討では,BNPが,問診や身体所見,X線所見等の診断パラメターのなかで最も有用であった61)(この研究ではBiosite製のBNP測定装置を用いてカットオフ値を設定しているが,シオノリアBNPとの換算式が確定していない現在では,その値を直接我が国にあてはめることはできない).血中BNP濃度はNew York Heart Association(NYHA)重症度分類に平行して上昇し,BNP値が高いほど心不全が存在し
重症である.
また,BNP濃度(NT-proBNPも含む)と予後の関係については,最初は重症心不全患者において報告され63),海外の大規模臨床試験のサブ解析においても確認
された64),65).重症慢性心不全患者を対象にARBの有用性を検討したVal-HeFT研究のサブ解析では,すべての症例をBNP値の低い順に4分割すると,BNPの高い群ほど心事故の発生率の高いことが示された.この研究での中央値は97 pg/mL(この研究ではシオノリアBNPで測定されており,我が国と同じ測定系である)であり,BNP値が10 pg/mL上昇するごとに死亡率が1.2%上昇することが報告されている64).また,慢性心不全患者を年間追跡した臨床研究では,ANP,BNP,ノルエピネフリン,臨床症状,血行動態所見を比較して,予後との関連を調べ,BNP濃度と肺動脈楔入圧のみがそれぞれ単独で予後規定因子であることが報告されている63).慢性心不全で入院した症例を対象に,退院時のBNP値で退院後の心事故(死亡,心不全の悪化による再入院)の発生率を前向きに比較検討すると,BNP値が低いほど有意に低率であり,およそ200~ 250 pg/mLが退院時のメルクマールになる66).さらには,外来通院中の安定した患者においては,190 pg/mL以上で心事故が増加する67).また,心筋梗塞後の患者においては180 pg/mL以上(約1か月の測定)で心臓死が増加すると報告されている68).
一般集団を対象にした健診におけるBNPの有用性に関しては未だ結論が出ていない.ただ,Framingham Studyでは集団の80パーセンタイル値(約20 pg/mL; シ
オノリアBNPで測定)以上の群では,以下の群より有意に心事故の発生率が高いことが示されている69).心不全の場合,陰性的中率が高いので,呼吸困難等で心不全を疑うべき症例において,BNP値が正常であれば,心不全である可能性は極めて低い.
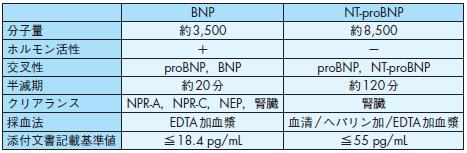
我が国では主にBNPの血中濃度が測定されているが,欧米ではBNP前駆体のNT-proBNPの測定系もよく利用されており,心不全の診断・予後診断にBNPとほぼ同等の結果が報告されている70),71).両者の特徴を表3に示すが,使い分ける際には注意が必要である.BNPには生理活性があり,NT-proBNPには生理活性が
ないこと,半減期が長いこと,腎機能の影響を受けやすいこと等が特徴である.
BNPやNT-proBNPを利用した心不全診断と重症度評価をする上での問題点は,年齢,性別,肥満,腎機能等の影響を受けることである.BNP,NT-proBNPの測定
系の世界的標準化とともにこれらの問題点解決が期待される.
④ その他の神経体液因子
1)エンドセリン
エンドセリン(ET)は1988年に血管内皮細胞培養上清中から発見された72)強力で,かつ持続的な血管平滑筋収縮性ペプチドである.エンドセリンは,構造と薬理活
性の異なる3種類のアイソペプチド,ET-1,ET-2,ET-3からなるETファミリーである.ET受容体にはET-1 選択性のET-A受容体,およびETアイソペプチド非選択性ET-B受容体がある.血管平滑筋にはET-A受容体が発現し,血管収縮に働く.一方,血管内皮細胞においては,ET-B受容体が発現してNOの放出に関与する.血管平滑筋にもET-B受容体が発現して収縮に関与するとされている.ET-B受容体はアルドステロンの分泌にも関与する73).
心不全の重症度が増すにつれて,血漿ET-1 濃度は高値を示すが74),特にNYHAの重症度分類Ⅳ度で上昇する.血漿ET-1,big-ET-1 濃度はLVEFとは逆相関して,死亡率の規定因子の1つである75)-77).慢性心不全患者を対象に,ACE阻害薬やβ遮断薬との併用でET受容体拮抗薬の有効性が検討されたが,現時点では予後改善効果はない.血中のET-1 は肺循環から,また末梢循環からも産生され,肺血管床ではET-1 の産生量と肺血管抵抗とは正の相関を示すことから,肺高血圧に関係している74).現在,肺動脈性肺高血圧症におけるET-A/B受容体拮抗薬,ボセンタンの臨床応用が可能であるが,心不全治療薬としては確立されていない.
2)アドレノメデュリン
アドレノメデュリン(AM)は,心不全の重症度が増すにつれて血中濃度は増加し,予後不良と関係する78).ANP,BNPに比較して79),心不全の重症度評価,治療
効果判定の指標にはなりにくい.AMはIL-1,TNF-α等のサイトカインにより分泌を刺激され,心臓のみならず全身の血管床から産生され,オートクリン,パラクリンに細胞保護的に働いている.AMは細胞内cAMPを増加することで,血管拡張作用,心機能改善作用,神経体液因子調節作用もあるので心不全治療薬として有用である
可能性がある78).
3)バゾプレッシン
バゾプレッシンは脳下垂体後葉から分泌されるホルモンで,心不全で上昇しV1受容体を介して血管収縮,V2受容体を介して体液調節をしている.バゾプレッシンの
前駆体のフラグメントであるコペプチン濃度は,心不全患者で予後と関連すると報告されている80).バゾプレッシン受容体の拮抗薬の臨床効果の検討がされた結果,V2受容体拮抗薬は,利尿効果において有用性が認められたが81),予後改善効果は認められなかった.
⑤ その他のバイオマーカー
1)心筋傷害マーカー
心筋梗塞のバイオマーカーでもある心筋特異的トロポニン(I,T)濃度が,虚血性心疾患でのリスク指標としての有用性は確立されているが,非虚血性心筋疾患でも
上昇することが指摘され,持続的な上昇が予後不良の指標となる可能性が指摘されている82)-84).最近,高感度トロポニン濃度測定系が,従来の測定系に比べて,急性冠症候群の診断に有用であるとの報告もあり85),86),その慢性心不全のリスク評価での有用性が期待される87),88).
2)炎症性マーカー
心不全の発症に免疫細胞,およびそれらが産生するサイトカインの関与が指摘されている89).実際,心不全患者においてtumor necrosis factor-α(TNF-α),Interleukin-6(IL-6)が血中に増加し,予後とも関係する90),91).これらのサイトカインは直接的な陰性変力作用,β受容体に対する反応抑制,一酸化窒素の産生を介する心筋細胞障害によって心機能を抑制する.さらに筋肉の疲弊を来たし心臓悪液質にも関与する.また血管の透過性亢進,末梢血管抵抗増大,心不全患者の運動耐容能低下にも関与する.TNF-α,IL-6等のサイトカイン以外にも可溶性サイトカイン受容体92)ならびに可溶性接着分子も増加している75).なかでも,高感度CRP濃度測定が基礎疾患の有無にかかわらず予後と関連しているとの報告がある93),94).高感度CRP測定は,サイトカインより簡便で,安価であるが特異性に欠ける.
3)酸化ストレスマーカー
心不全では,酸化ストレスが亢進し,内皮障害や心機能障害増悪の要因とされる.その指標として,血中酸化LDL濃度95),96), 血中- 尿中8-iso-prostaglandin PGF2α(isoprostane)97),や8-OH-deoxyguanosine98),99)等が報告されている.酸化ストレス亢進は,交感神経系やRAA系,炎症性反応等の経路の下流に位置すると考えらるが,多臓器不全を合併する心不全では,その由来細胞や臓器が特定できない点が問題である.尿酸高値は,非特異的な指標ではあるが,簡便な酸化ストレスマーカーとして有用である可能性がある100)-102).
4)アディポサイトカイン
メタボリック症候群は,虚血性心疾患の危険因子であり心不全のリスクでもある.メタボリック症候群関連アディポサイトカインの1つであるアディポネクチン濃度は心不全で上昇し,予後と関連すると報告されている103)-105).アディポネクチンには,抗動脈硬化作用,インスリン抵抗性改善作用があり,心不全のない患者においてはアディポネクチン低値が心筋梗塞発症のリスクとされる.一方,心筋梗塞や心不全を発症するとアディポネクチン濃度は上昇し,予後不良の指標となる.この現象
は,肥満が心不全のリスクであるが,心不全患者において肥満患者の予後は比較的良好で,やせ(悪液質)患者で予後不良である(オベシティパラドックス)のと似た現象である.
神経体液因子の評価
ClassⅠ
● 血漿BNP濃度測定:診断,重症度,予後評価
ClassⅡ a
● 血漿BNP濃度測定:治療効果判定
● NT-proBNP濃度測定:診断,重症度,予後評価
● 血漿ノルエピネフリン濃度測定:重症度,予後評価
● 心筋トロポニン濃度測定:重症度,予後評価
● 血漿ANP濃度測定
● 血漿レニン活性値,または濃度測定
● 血漿アルドステロン濃度測定
ClassⅡb
● NT-proBNP濃度測定:治療効果判定
● 血漿BNP濃度やNT-proBNP濃度測定:スクリーニング目的として
ClassⅢ
● スクリーニング目的での神経体液因子(血漿BNP濃度,NT-proBNP濃度を除く)
表3 BNPとNT-proBNPの特徴
Ⅰ 慢性心不全病態と診断 >
3 神経体液因子 >
1 慢性心不全と神経体液因子
慢性心不全治療ガイドライン(2010年改訂版)
Guidelines for Treatment of Chronic Heart Failure(JCS 2010)
Guidelines for Treatment of Chronic Heart Failure(JCS 2010)